FDA przyznała firmie Suzhou CH Biomedical zgodę na rozpoczęcie badań klinicznych nad systemem wspomagania lewej komory serca BrioVAD™, obiecując innowacyjne rozwiązania w leczeniu niewydolności serca.


Niedawno firma Suzhou CH Biomedical, Inc. ogłosiła, że jej samodzielnie opracowany, w pełni magnetycznie lewitujący system wspomagania lewej komory serca BrioVAD™ otrzymał zgodę amerykańskiej FDA na przeprowadzenie badań klinicznych. Przełomowe badanie kliniczne, nazwane INNOVATE, uzyskało od FDA zgodę na stosowanie urządzeń eksperymentalnych (IDE), co pozwala na warunkowe rozpoczęcie rekrutacji pacjentów.
Badanie to oceni skuteczność i bezpieczeństwo systemu BrioVAD™, nowego w pełni magnetycznie lewitującego systemu wspomagania lewej komory serca opracowanego przez CH Biomedical, w leczeniu opornej niewydolności serca. Tymczasem firma CH Biomedical zwołała pierwsze spotkanie badaczy tego badania i rozpoczęła prace nad otwarciem ośrodków badań klinicznych w Stanach Zjednoczonych.

▲ CH Biomedical organizuje pierwsze spotkanie badaczy w ramach badania INNOVATE
System wspomagania lewej komory serca BrioVAD™, zatwierdzony przez FDA w Stanach Zjednoczonych, opiera się na doskonałej kompatybilności krwi z istniejącym produktem CH-VAD. Dzięki kilku innowacjom technologicznym osiąga przenośność zewnętrznych komponentów noszonych, jednocześnie zwiększając ogólną wydajność systemu. Ponadto w badaniu INNOVATE zastosowany zostanie randomizowany projekt kontrolowany w celu porównania i oceny systemu BrioVAD™ z wcześniej zatwierdzonymi przez FDA produktami.
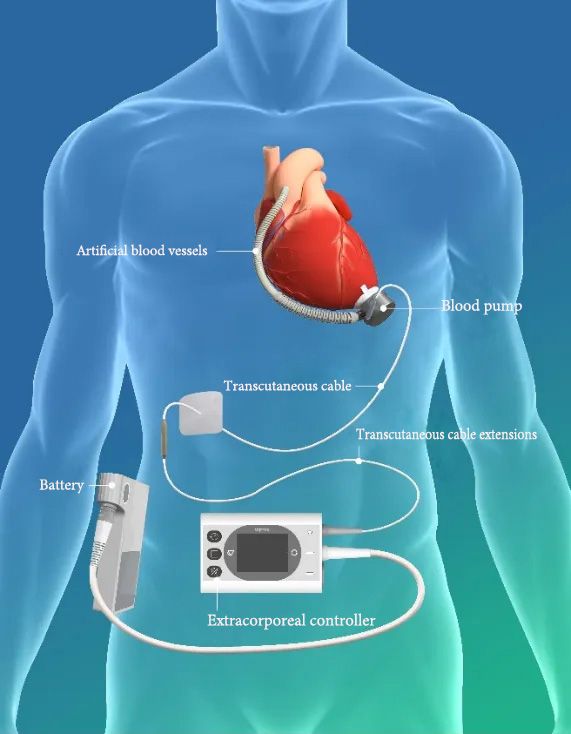
▲ Schemat produktu systemu wspomagania lewej komory serca BrioVAD™
CH-VAD to pierwszy w pełni magnetycznie lewitujący, implantowany system wspomagania lewej komory serca (LVAD) opracowany w Chinach. Opracowany wspólnie przez zespół z Fuwai Hospital i CH Biomedical, waży 186g, ma średnicę pompy krwi wynoszącą 50mm, grubość 26mm i maksymalny przepływ 10L/min. Główna technologia tego produktu polega na w pełni magnetycznie lewitującej technologii pompy krwi, która uzyskała wiele patentów w Chinach i Stanach Zjednoczonych, czyniąc go pionierskim urządzeniem medycznym w kraju. W porównaniu do podobnych produktów międzynarodowych, jego kluczowe wskaźniki wydajności osiągnęły ten sam poziom, przy mniejszych rozmiarach pompy i lepszej inwazyjności implantu.
CH-VAD jest klinicznie dostępny od 2018 roku i otrzymał zgodę NMPA na stosowanie ze specyficznymi sztucznymi naczyniami krwionośnymi w 2021 roku, zapewniając wsparcie mechaniczne dla krążenia krwi u pacjentów z końcową niewydolnością serca, stosowany jako terapia przejściowa przed przeszczepem serca lub w celu odzyskania funkcji serca.

▲ Implantowany system wspomagania lewej komory serca CH®
CH-VAD składa się z wewnętrznych komponentów implantowanych, zewnętrznych komponentów noszonych, komponentów peryferyjnych oraz specjalistycznych narzędzi chirurgicznych. Jest to urządzenie zintegrowane elektromechanicznie, używane do częściowego zastąpienia funkcji pompowania serca i utrzymania krążenia krwi. Jego kluczowym komponentem jest pompa krwi, która pobiera krew z serca, zwiększa jej ciśnienie i dostarcza do aorty, odciążając naturalne serce, umożliwiając mu odpoczynek, a jednocześnie uzupełniając niedostateczną zdolność pompowania naturalnego serca.
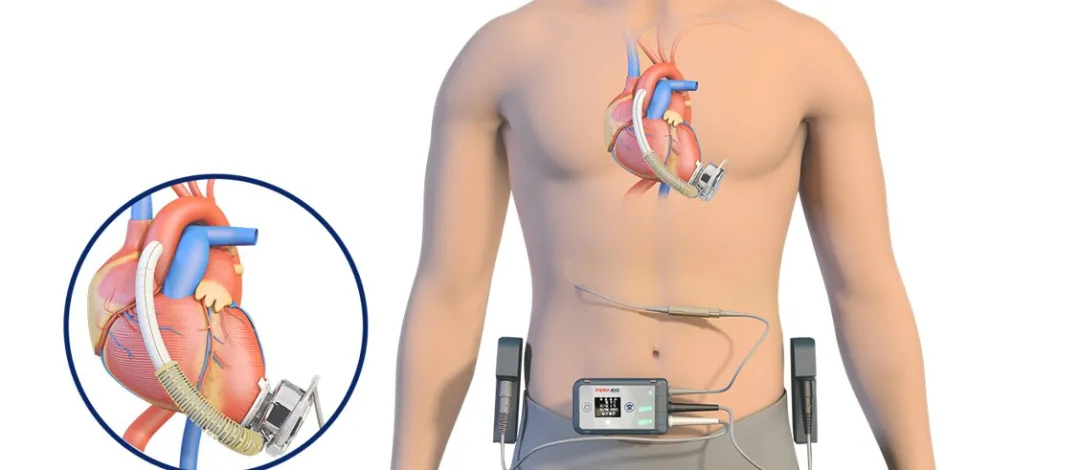
▲ Implantowany system wspomagania lewej komory serca CH®
Od momentu wprowadzenia na rynek, CH-VAD został zastosowany u ponad 180 pacjentów w ponad 40 czołowych ośrodkach kardiologicznych w całym kraju. Pierwszy pacjent przeżył ponad 6 lat i nadal prowadzi wysokiej jakości życie. CH-VAD posiada pełny system niezależnych praw własności intelektualnej, zbudowany od podstaw i uzyskał ochronę patentową w Chinach, Stanach Zjednoczonych, Europie, Japonii i innych krajach i regionach.
W kwietniu 2024 roku, na sympozjum ISHLT "Spin Doctors and Heart Hotties: Unleashing the Future of MCS Devices", profesor Xianqiang Wang z Fuwai Hospital, Chińskiej Akademii Nauk Medycznych, przedstawił długoterminowe wyniki obserwacji CH-VAD na arenie międzynarodowej. W tym jednoośrodkowym, retrospektywnym, obserwacyjnym badaniu, pacjenci z końcową niewydolnością serca leczeni CH-VAD wykazali wysokie wskaźniki przeżycia i niskie wskaźniki powikłań, bez przypadków zakrzepicy pompy, udarów inwalidujących ani poważnych awarii urządzenia.
Cele badania
Aby dalej ocenić długoterminową skuteczność i bezpieczeństwo CH-VAD, Fuwai Hospital przeprowadził to jednoośrodkowe, retrospektywne, obserwacyjne badanie, obejmujące pacjentów z niewydolnością serca leczonych CH-VAD od czerwca 2017 do sierpnia 2023, w celu statystycznej analizy ich danych klinicznych i długoterminowych prognoz.
Metody badawcze
W badaniu uwzględniono 50 pacjentów, z okresami obserwacji od 3 miesięcy do 6,7 lat. Średni czas wsparcia pompy dla pacjentów wynosił 2,4 roku, a wszyscy 50 pacjentów pomyślnie przeszło implantację LVAD. Operacja pompy krwi była stabilna zarówno podczas operacji, jak i po niej, a hemodynamika wróciła do normy.
Wyniki badania
Stosując analizę przeżycia Kaplan-Meier, roczne, dwuletnie i trzyletnie wskaźniki przeżycia pacjentów wynosiły odpowiednio 93%, 93% i 89%, wszystkie wyższe niż w międzynarodowych badaniach klinicznych i rzeczywistych warunkach. Spośród 50 pacjentów, tylko 2 przeszło przeszczep serca jako pomost. Trzech pacjentów całkowicie odzyskało funkcję serca i usunięto LVAD.
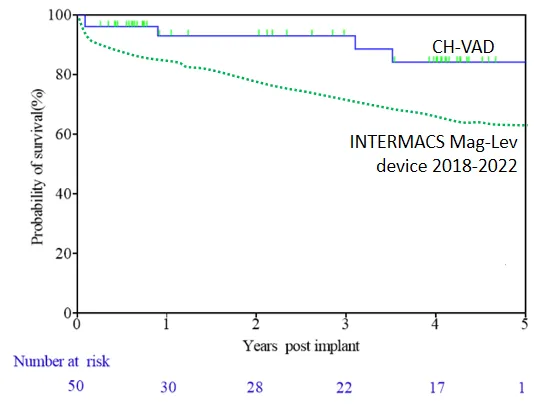
▲ Przeżywalność pacjentów podczas obserwacji
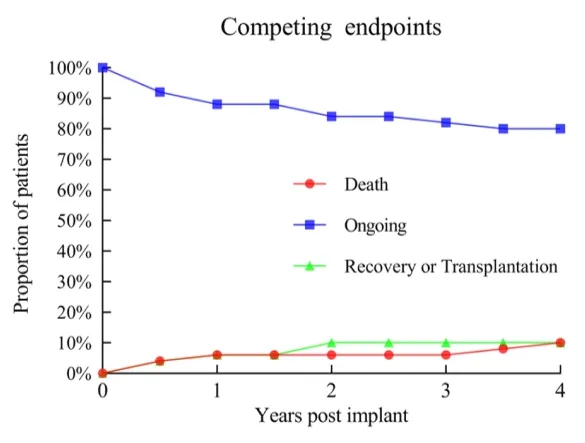
▲ Występowanie zdarzeń dla różnych punktów końcowych
W tym badaniu ogólny wskaźnik występowania zdarzeń niepożądanych był niski. Doskonała kompatybilność krwi CH-VAD była widoczna, bez obserwowanych przypadków zakrzepicy pompy, hemolizy ani inwalidujących zdarzeń udarowych.
Spośród wszystkich pacjentów, tylko 2 doświadczyło udarów niedokrwiennych (0,02 na osobę-roku), a 1 doświadczył udaru krwotocznego (0,01 na osobę-roku), przy czym wszystkie funkcje neurologiczne pacjentów wróciły do normy podczas obserwacji. Najczęstszym zdarzeniem niepożądanym była infekcja pooperacyjna, która była skutecznie zapobiegana i kontrolowana dzięki doświadczeniu w zarządzaniu interdyscyplinarnym, prowadząc do dobrego rokowania u większości pacjentów. Nie było żadnych poważnych awarii urządzeń ani operacji wymiany pomp podczas okresu obserwacji, co wskazuje na wysoką długoterminową niezawodność urządzenia.
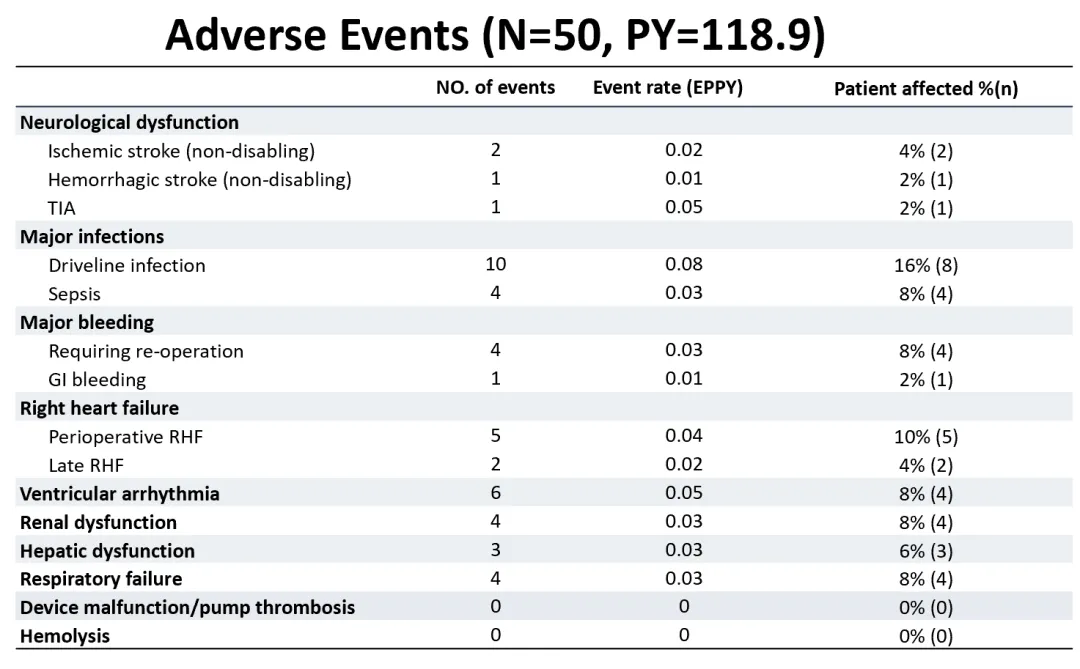
▲ Występowanie różnych typów zdarzeń niepożądanych
15 kwietnia 2024 roku, Amerykańska Agencja Żywności i Leków (FDA) ogłosiła wycofanie systemów wspomagania lewej komory serca HeartMate II i HeartMate 3 firmy Abbott/Thoratec z powodu wystąpienia zjawiska "Entrinsic Outflow Graft Obstruction" (EOGO) spowodowanego siłami zewnętrznymi. To wycofanie dotyczyło 13 883 urządzeń, co stanowi 56% wszystkich produktów rynkowych, z oszacowanym przez Kaplan-Meier wskaźnikiem wystąpienia wynoszącym 0,24% po 2 latach i 2,06% po 5 latach dla EOGO HeartMate 3.
Incydenty EOGO związane z HeartMate II i HeartMate 3 w tym wycofaniu nie są nowe w branży. Do tej pory FDA otrzymała liczne zgłoszenia o zdarzeniach niepożądanych związanych z EOGO z HeartMate, obejmujących 273 przypadki urazów i 14 przypadków śmierci.
Warto zauważyć: Po pierwsze, wycofanie urządzeń klasy I przez FDA nie oznacza zaprzestania produkcji ani użytkowania produktu, lecz podjęcie działań korygujących w celu rozwiązania zidentyfikowanych problemów, a urządzenia będą nadal używane w warunkach klinicznych. Po drugie, przyczyną wycofania klasy I HeartMate II i HeartMate 3 przez FDA jest EOGO, które jest spowodowane gęstą powłoką wzmacniającą z materiału PTFE HeartMate II i HeartMate 3, co skutkuje gromadzeniem się eksudowanych materiałów niekomórkowych, zmuszając sztuczne naczynie krwionośne do skurczenia się. Jednak krajowe urządzenia LVAD, reprezentowane przez CH-VAD, rozwiązały powyższe wady konstrukcyjne HeartMate dzięki wydrążonej konstrukcji powłoki wzmacniającej.
Technologia magnetycznej lewitacji umożliwia stabilne obracanie się bez potrzeby stosowania cieczy, co znacznie zmniejsza uszkodzenia krwi, a tym samym zmniejsza występowanie związanych z tym powikłań, takich jak zakrzepica i udar. CH-VAD osiąga stabilne zawieszenie w pięciu stopniach swobody na osiach X, Y i Z poprzez umieszczenie statora silnika i statora lewitacji magnetycznej po wewnętrznej i zewnętrznej stronie wirnika, zapewniając dobrą odporność na wstrząsy i stabilną długoterminową pracę, zmniejszając uszkodzenia krwi. Jednocześnie zoptymalizowany projekt kanału przepływu zapewnia płynny przepływ krwi od rurki wlotowej do pozycji wirnika za pomocą stożka nosowego, z U-kształtnym wtórnym kanałem przepływu o szczelinie 250μm, zapewniając zarówno płynny przepływ krwi, jak i dobre efekty płukania.
Profesor Zengsheng Chen z Uniwersytetu Beihang podkreślił, że "winowajcą" tego wycofania jest gęsta powłoka wzmacniająca z materiału PTFE HeartMate II i HeartMate 3, podczas gdy krajowe urządzenia LVAD, reprezentowane przez CH-VAD, rozwiązały problem skurczenia się sztucznego naczynia poprzez wydrążoną konstrukcję powłoki wzmacniającej.
Dzisiejsze VAD to nowoczesne implantowane pompy. Przykładem może być CH-VAD, wyposażony w wyjątkowy wirnik, jeden ruchomy element, który efektywnie napędza krew w jednym kierunku. Zawieszony na magnesach, wirnik działa bez tarcia i nie ma elementów podatnych na zużycie.
Wirniki odgrywają kluczową rolę w VAD. Kiedy prąd przepływa przez magnesy, wirnik zaczyna się obracać. Krew jest wciągana do środka wirnika pod ciśnieniem ujemnym, a jego obracające się łopatki szybko przyspieszają krew od środka do zewnętrznych krawędzi. Ta przekształcona krew, teraz pod ciśnieniem dodatnim, wypływa z pompy przez dyszę wylotową do kaniuli wyjściowej.
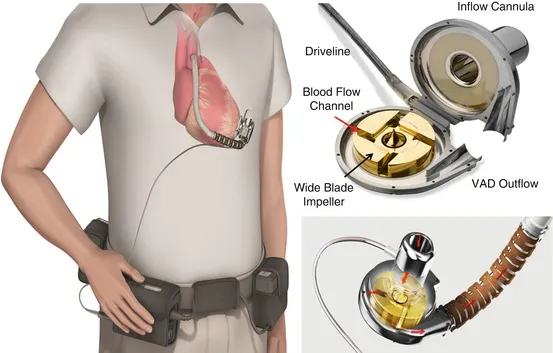
▲ Wirnik pompy krwi w VAD
Projekt wirnika jest kluczowy. Utrzymywany w miejscu przez magnesy i specjalistyczne łożyska, obraca się gładko bez dotykania boków. Taki projekt minimalizuje uszkodzenia i zapewnia długowieczność urządzenia.
W Manners Technology specjalizujemy się w tworzeniu części do urządzeń medycznych, w tym wirników do VAD. Nasze zaangażowanie w jakość potwierdzają nasze certyfikaty, w tym ISO 9001:2015 i ISO 13485.
Współpracujemy również z wiodącą niemiecką firmą w celu opracowania jeszcze bardziej wydajnych i niezawodnych wirników do VAD. Wspólnie dążymy do produkcji części, które przewyższają oczekiwania. Niezależnie od tego, czy potrzebujesz specjalistycznych części, czy pomocy w projektowaniu, nasze usługi dostosowane są do Twoich potrzeb.